Tablica z charakterystycznymi danymi
Liczba elektronów: 6
Liczba neutronów: 6
Liczba protonów: 6
Elektroujemność (Allred-Rochow, Pauling): 2.50, 2.55
Przewodność elektryczna: 1*1051/(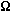 *m)
*m)
Gęstość (293K): 2.26 g/cm3
Temperatura topnienia: 3500°C, 3773 K
Temperatura wrzenia: 4827°C, 5100 K
Przewodność cieplna: 0.00129 W/(m*K)
Ciepło topnienia: --
Ciepło parowania: 355.8 kJ/mol

